ביוכימיה/מטענים
קפיצה לניווט
קפיצה לחיפוש
מטען של פפטיד
מטען הקצה הקרבוקסילי והקצה האמיני בתנאי pH שונים
pH הוא מדד לקביעת ריכוז יוני הידרוניום () בתמיסה. כל חומצה אמינית משמשות כחומצה (משחררות H) וכבסיס (קושרות H). באופן כללי, כאשר :
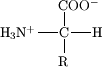
- pH חומצי – יש הרבה מימנים (H). כלומר המבנה של החומצה האמינית יהיה:
- קבוצה קרבוקסילית תראה כך : .
- קבוצה אמינית תראה כך : .
- pH בסיס – יש מעט מימנים. כלומר המבנה של החומצה האמינית יהיה:
- קבוצה קרבוקסילית תראה כך : .
- קבוצה אמינית תראה כך : .
טבלה מסכמת
 |
||
|---|---|---|
| סביבה בסיסית | סביבה נטרלית | סביבה חומצית |
| מעט | נטרלי | הרבה |
| חומצה אמינית מתנהגת כחומצה. | חומצה אמינית מתנהגת פעם כחומצה ופעם כבסיס. כלומר, היא ציווטריון, יון כפול; 2 הקבוצות טעונות בטורות.
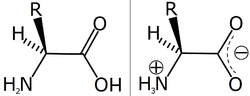 |
חומצה אמינית מתנהגת כבסיס. |
מושגים
- pI = pH אופטימלי = pH איזו אלקטרי – ה-pH בו ערך כלל המטענים בחומצה האמינית שווים לאפס. לכל חומצה pI משלה. כאשר :
- - החומצה שלילית.
- - החומצה חיובית.
- - כלל המטענים בחומצה שווים לאפס.
- pH פיזיולוגי - pH שקיים בגוף, נקבע כ-7.4.
מטען של חומצה אמינית
מושגים PKA, PKB, PKR
- PKa – ערך ה-pH בו 50% מהמולקולות טעון בקבוצה קרבוקסילית ו-50% לא.

- PKb – ערך ה-pH בו 50% מהמולקולות טעון בקבוצה האמינית ו-50% לא.
- PKR – ערך ה-pH בו 50% מחומצות האמינו בשייר טעונות ו-50% לא.
- PI – ערך כלל המטענים שווה לאפס.
חוקים לקביעת PI של ח.א
- חומצות שאינן מתיינות (אין מטענים) בכלל :
- חומצות אמינו שמתיינות בקבוצה קרבוקסילית (גלוטמית ואספרטית) :
- חומצות אמינו שמתיינות בקבוצה האמינית (לאה – ליזין, ארגנין והיסטדין) :
- ח.א שמתיינות באופן שונה (ציסטאין וטירוזין) :